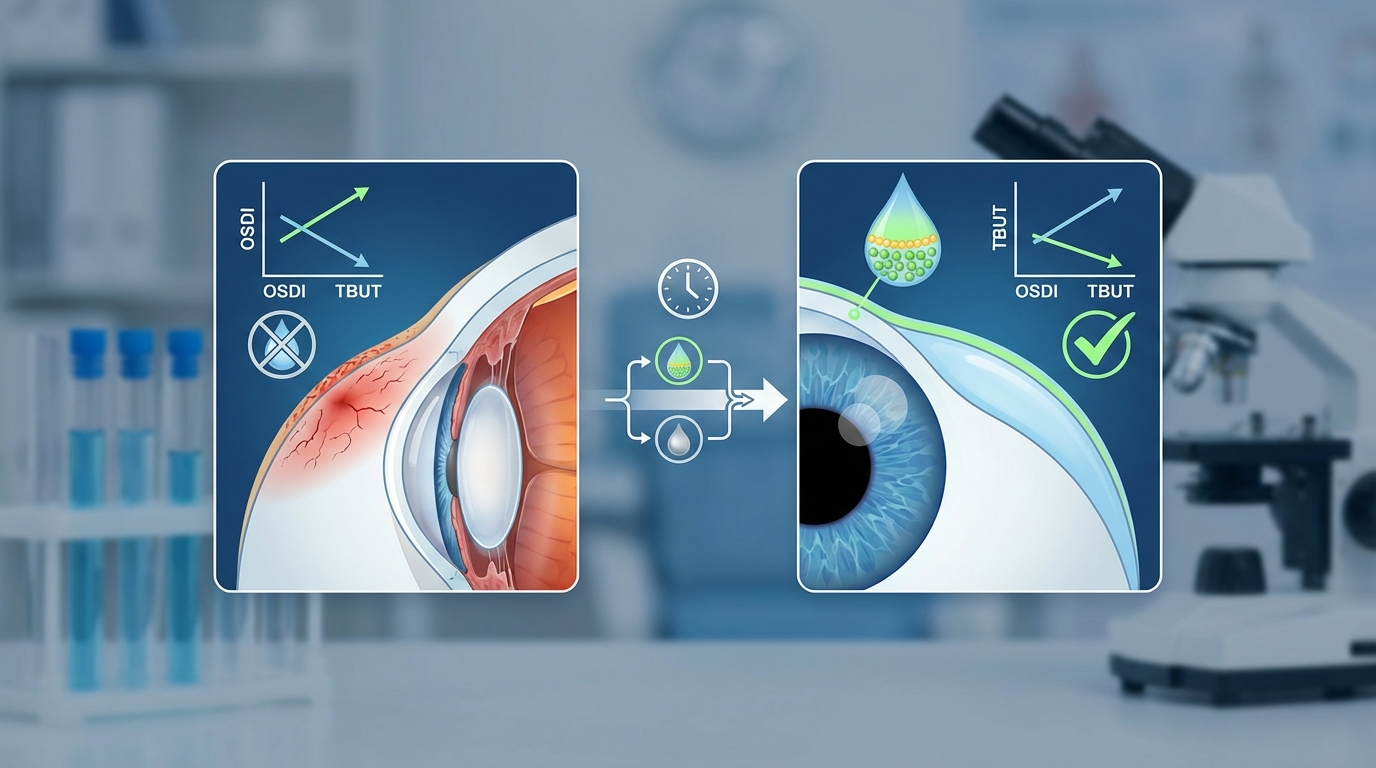
Новые клинические данные по препарату для лечения умеренным и тяжёлым синдромом "сухого глаза"
Введение
Научный и клинический фон
Синдром сухого глаза (Dry Eye Disease, DED) остаётся распространённой проблемой офтальмологии, затрагивающей значительную долю населения во всем мире. Рост продолжительности работы за экранами и ухудшение качества внешней среды повышают частоту проявлений. В арсенале терапии — увлажняющие капли, коррекция функции мейбомиевых желёз, противовоспалительная терапия; однако у части пациентов контроль симптомов недостаточен, а вещества вызывают побочные эффекты или неудовлетворительный ответ.
Разработка липидных или мультикомпонентных формул, имитирующих естественную слёзную плёнку, направлена на восстановление стабильности слёзной плёнки и снижение испарения слёз.
Дизайн исследования
- Тип: рандомизированное, двойное слепое, плацебо‑контролируемое исследование
- Выборка: 320 пациентов с умеренной и тяжёлой формой синдрома сухого глаза (OSDI ≥ 23)
- Рандомизация: экспериментальная группа (новая липидная искусственная слеза) vs контроль (плацебо)
- Продолжительность лечения: 12 недель
- Основные конечные точки:
- OSDI (индекс поражения поверхности глаз) — субъективная симптоматика
- TBUT (время разрыва слезной пленки) — стабильность слёзной плёнки
- Кодирование флюоресцеиновой окраски роговицы — структурные изменения
- Вспомогательные конечные точки: безопасность, качество жизни пациентов
Результаты
- Эффективность:
- В экспериментальной группе средний OSDI снизился с 45,2 ± 10,3 до 22,1 ± 8,7 (P < 0,001), что демонстрирует выраженное клиническое улучшение симптомов.
- В контрольной группе итоговый OSDI составил 38,5 ± 9,8; изменение по сравнению с исходным уровнем не было статистически значимым (P = 0,12).
- TBUT в экспериментальной группе увеличился с 5,6 ± 1,2 с до 9,8 ± 2,1 с (P < 0,001), что указывает на восстановление стабильности слёзной плёнки.
- Улучшение флюоресцеиновой окраски коррелировало с клиническими показателями в группе лечения.
- Безопасность:
- Серьёзных нежелательных явлений не зарегистрировано.
- Лёгкие местные симптомы отмечены у менее чем 5% пациентов и носили транзиторный характер.
- Вывод авторов: препарат демонстрирует значимое улучшение симптоматики и объективных признаков DED при благоприятном профиле переносимости.
Обсуждение и клинические замечания
Новая формула содержит липидный компонент, имитирующий слоистую структуру натуральной слёзной плёнки, что объясняет улучшение TBUT и уменьшение субъективных симптомов. Особенно перспективным выглядит применение у пациентов с мейбомиевой дисфункцией и повышенным испарением слёзной плёнки.
Ключевые клинические соображения:
- Результаты получены в 12‑недельном периоде; требуется длительное наблюдение для оценки устойчивости эффекта и безопасности.
- Необходимы дополнительные исследования с увеличенной выборкой и анализом подгрупп (например, разные фенотипы DED, коморбидности).
- После регистрации препарата важно организовать пострегистрационный мониторинг и фармаконадзор для выявления редких и отсроченных побочных эффектов.
Практические рекомендации при внедрении (при условии регистрациi)
- Следовать национальным регистрационным требованиям и инструкциям по применению, утверждённым регулятором.
- Подбирать терапию с учётом фенотипа сухого глаза (мейбомиевая дисфункция, гиперосмолярность и т.д.).
- Информировать пациентов о статусе препарата (исследуемый/зарегистрированный), о возможных побочных реакциях и необходимости сообщать о них для фармаконадзора.
- Вести документацию и согласия в соответствии с требованиями законодательства об охране здоровья и защите персональных данных.
Ограничения исследования
- Короткий интервал наблюдения (12 недель).
- Необходимость подтверждения результатов в популяциях с иным генетическим и экологическим бэкграундом.
- Требуется информация о взаимодействии с другими офтальмологическими препаратами и о влиянии на подтипы DED.
Юридические и этические аспекты
Информация в этом материале носит обзорный и научный характер. До официальной регистрации и включения в инструкцию по медицинскому применению любое использование препарата должно соответствовать Федеральному закону № 61‑ФЗ «Об обращении лекарственных средств», требованиям Федерального закона № 323‑ФЗ «Об основах охраны здоровья граждан в Российской Федерации», а также нормам по защите персональных данных (ФЗ‑152). Необходимо организовать информированное согласие пациентов и обеспечить надлежащую информбезопасность медицинских данных.
Заключение
Многоцентровое рандомизированное исследование демонстрирует перспективный профиль эффективности и безопасности новой липидной искусственной слёзы у пациентов с умеренной и тяжёлой формой DED. Для интеграции в клиническую практику требуются регистрационные процедуры, дальнейшие длительные исследования и организационная подготовка по фармаконадзору.
Источники
- Zhang S et al. Advances in Dry Eye Treatment. Chinese Journal of Ophthalmology, 2025; 61(12): 1123–1130.
Примечание: исходный материал — онлайн‑версия Chinese Journal of Ophthalmology, опубликовано 15 декабря 2025 г. Представленные здесь данные отражают результаты исследования и не заменяют официальные инструкции по применению лекарственных средств после регистрации. При работе с пациентами руководствуйтесь текущим нормативным регулированием и локальными протоколами оказания медицинской помощи.